K바이오주 셀트리온 '트룩시마' 美 판매허가
이태영 KB증권 연구원 "독보적 지위 전망"
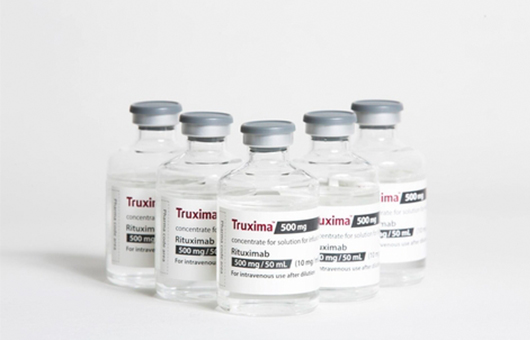
[FE금융경제신문=이도희 기자] 셀트리온의 미국 바이오의약품 시장 공략이 본격화되고 있다. 앞서 셀트리온은 미국 식품의약국(FDA)으로부터 트룩시마의 최종 판매 허가를 획득했다고 29일 공시했다.
◇K바이오주 셀트리온 '트룩시마' 美 판매허가
자가면역질환 항체 바이오시밀러(바이오의약품 복제약) 램시마에 이어 혈액암 항체 바이오시밀러 트룩시마까지 미국 의약품 허가장벽을 넘어선 것이다. 셀트리온은 이번 트룩시마의 허가획득으로 미국 시장 진입 속도가 더욱 빨라질 것으로 예상했다.
특히 리툭시맙 바이오시밀러 경쟁자인 산도스가 미국 시장 진출 포기 선언함에 따라 셀트리온은 경쟁자 없이 5조원 규모의 미국 리툭시맙 시장 선점이 가능해졌다.
셀트리온은 트룩시마의 오리지널 의약품인 '맙테라·리툭산(성분명 리툭시맙, 판매사 로슈)'과의 경쟁에서도 자신감을 보였다. 자가면역질환 치료제 시장과 달리 항암제 시장은 미국 보험사 진입에 제한이 없기 때문이다.
미국에서 의료보험 혜택을 받기 위해서는 공보험, 또는 사보험에 가입해야 하고, 환자는 각각의 보험사에서 제공하는 의약품 급여 목록 내에서 처방을 받을 수 있다. 램시마가 미국 출시 당시 부진한 성적을 거둔 이유도 미국 보험사 진입에 실패했기 때문이다.
당시 오리지널사인 존슨앤존슨은 미국 사보험사들과 '패키지 판매(두 개 이상의 제품을 특정 가격에 묶어 판매)' 계약을 1년~3년치 미리 맺는 전략을 구사해 램시마의 보험사 진입을 막은 바 있다.
김형기 셀트리온헬스케어 대표는 "항암제는 사람의 생명과 직결된 의약품"이라며 "램시마때처럼 오리지널사가 리베이트(보험사·병원 등에 일정 부분 이익을 제공하는 금액) 전략으로 보험사 진입을 막기 어려울 것"이라고 설명했다.
그는 "미국 항암제 분야에서 강력한 마케팅 네트워크를 구축한 테바와 파트너십을 맺었다"며 "트룩시마는 이들의 네트워크를 활용해 램시마보다 더욱 빠른 속도로 성장할 수 있을 것"이라고 덧붙였다.
미국 정부가 예고한 바이오시밀러 확대 정책도 트룩시마의 시장 진입과 매출 확대에 큰 도움이 될 것으로 보인다.
미국 정부는 최근 △바이오시밀러의 개발 및 승인과정 효율화 △바이오시밀러 이해도를 높이기 위한 환자, 의사, 보험사와의 효율적 커뮤니케이션 △공정한 시장경쟁 장려 등을 주요 골자로 한 바이오시밀러 육성정책(BAP, Biosimilars Action Plan)을 통해 바이오시밀러 도입과 경쟁을 촉진하겠다는 뜻을 밝힌 바 있다.
김 대표는 "항체 바이오시밀러로는 세계 최초로 FDA의 허가를 받고 미국 시장에 진입한 램시마에 이어 트룩시마까지 경쟁사들보다 빠른 속도로 시장에 선보임으로써 퍼스트무버 지위를 누리게 됐다"며 "미국 정부의 바이오시밀러 육성정책에 힘입어 내년부터 미국 시장에서의 제품 성장세가 본격화 될 것"이라고 말했다.
◇이태영 KB증권 연구원 "독보적 지위 전망"
이태영 KB증권 연구원은 "트룩시마는 유럽시장에서 지난 2017년 4월 첫 출시 이후 폭발적으로 점유율을 확대, 지난 2분기 기준 출시 국가 18곳에서 32%에 달하는 점유율 달성했다"며 "더군다나 주요 경쟁사였던 산도즈가 미국 출시 포기를 선언함에 따라 초기 선점이 중요한 바이오시밀러시장에서 독보적인 위치를 차지할 것"이라고 내다봤다.
또 "현재 트룩시마의 가장 가까운 경쟁자로는 화이자의 'PF-05280586'이 있는데 지난 9월에서야 FDA에 허가를 신청했다"며 "이에 따라 화이자가 허가받을 것으로 예상되는 시기는 내년 3분기로 트룩시마와의 진출 시점 격차가 최소 7개월 이상 발생한다"고 설명했다.